لوحة تميز المدونة
بعد الانتهاء من عرض المدونة التي شرحت
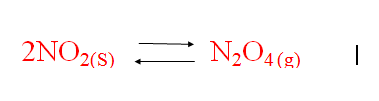
( وحدة التفاعلات والحسابات الكيميائية )
للصف الاول ثانوي العلمي بطرق مبسطة وسلسلة تسهل وصول المعلومه الى الذهن ومزج الدراسة في حدود التشويق , سندرج هنا اسماء افضل ثلاث طالبات في الاداء طيله مدة تدريس المدونه
الطالبة الاولى : ...............................................
الطالبة الثانية : ................................................
الطالبة الثالثة : .................................................
( وحدة التفاعلات والحسابات الكيميائية )
للصف الاول ثانوي العلمي بطرق مبسطة وسلسلة تسهل وصول المعلومه الى الذهن ومزج الدراسة في حدود التشويق , سندرج هنا اسماء افضل ثلاث طالبات في الاداء طيله مدة تدريس المدونه
فقط ......
عندما يكون للإبداع معنى....
عندما تكون لثقة كلمه......
عندما يكون للجهد شكر....
عندما يكون للفرد هدف....
عندما يكون للرقى سطور ....
فانني هنا اسطر مدى اعجابي بالطالبات اللواتي تميزن بالتفاعل العالي ⇣
الطالبة الاولى : ...............................................
الطالبة الثانية : ................................................
الطالبة الثالثة : .................................................